Table of Contents
I. Tính chất vật lí của axetilen
Axetilen là chất khí, không màu, không mùi, ít tan trong nước, nhẹ hơn không khí (d =
Hình 1. Thu axetilen bằng cách đẩy nước.
II. Cấu tạo phân tử của axetilen
Công thức cấu tạo: H – C ≡ C – H, viết gọn HC ≡ CH

Hình 2. Mô hình phân tử axetilen.
Phân tử có một liên kết ba, trong đó có hai liên kết kém bền, dễ đứt lần lượt trong các phản ứng hóa học.
III. Tính chất hóa học của axetilen
1. Axetilen có cháy không?
Hiện tượng: Axetilen cháy trong không khí với ngọn lửa sáng, tỏa nhiều nhiệt
PTHH: 2C2H2 (k) + 5O2 (k)
2. Axetilen có làm mất màu dung dịch brom không?
Hiện tượng: Axetilen làm mất màu dung dịch brom.
PTHH:
CH ≡ CH (k) + Br – Br (dd) → Br – CH = CH – Br (l)
màu da cam không màu

Hình 3. Axetilen tác dụng với dd brom.
Sản phẩm sinh ra có liên kết đôi nên có thể cộng tiếp với một phân tử brom nữa:
Br – CH = CH – Br (l) + Br – Br (dd) → Br2CH – CHBr2 (l)
* Trong điều kiện thích hợp, axetilen cũng có phản ứng cộng với hiđro và một số chất khác.
IV. Ứng dụng của axetilen
Dùng làm nhiên liệu trong đèn xì oxi - axetilen (nhiệt độ ngọn lửa có thể lên tới 3000oC)
Trong công nghiệp, axetilen là nguyên liệu để sản xuất poli(vinyl clorua) – dùng sản xuất nhựa PVC, cao su, axit axetic,…

Hình 4. Dùng đèn xì để hàn cắt kim loại
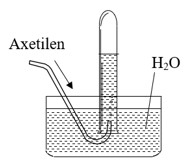
V. Điều chế axetilen
Cho canxi cacbua (thành phần chính của đất đèn) phản ứng với nước.
PTHH: CaC2 + 2H2O → C2H2 + Ca(OH)2
Phương pháp hiện đại: nhiệt phân metan ở nhiệt độ cao

Hình 5. Điều chế và thu khí axetilen trong phòng thí nghiệm
Bài tập axetilen của trường Nguyễn Khuyến
1. Tự luận
Câu 1: Viết phương trình hóa học của phản ứng xảy ra khi:
a) Dẫn axetilen qua ống thủy tinh đầu vuốt nhọn rồi đốt cháy khí axetilen thoát ra.
b) Dẫn axetilen qua dung dịch brom.
ĐÁP ÁN
a) 2C2H2 + 5O2
b) C2H2+ 2Br2 → C2H2Br4
Câu 2: Viết phương trình hóa học điều chế axetilen từ đất đèn (thành phần chính là canxi cacbua).
ĐÁP ÁN
PTHH: CaC2 + 2H2O → C2H2 + Ca(OH)2
Câu 3: Trình bày phương pháp hóa học phân biệt khí metan và khí axetilen. Viết phương trình hóa học của phản ứng xảy ra.
ĐÁP ÁN
Dùng dung dịch brom: Cho lần lượt từng khí trên vào dung dịch brom, khí nào làm mất màu dung dịch brom là axetilen, khí còn lại không có hiện tượng gì là metan.
PTHH: C2H2 + 2Br2 → C2H2Br4
Câu 4: Cho 5,6 lít hỗn hợp khí gồm metan và axetilen đi qua dung dịch brom dư, thấy dung dịch brom nhạt màu dần và có 1,12 lít khí thoát ra. Các thể tích khí đo ở điều kiện tiêu chuẩn. Tính thành phần phần trăm thể tích mỗi khí trong hỗn hợp ban đầu.
ĐÁP ÁN
PTHH: C2H2 + 2Br2 → C2H2Br4
Khí thoát ra là metan (không phản ứng với dung dịch brom).
2. Trắc nghiệm
Câu 1: Tính chất vật lí nào sau đây của axetilen là không đúng?
A.Là chất khí.
B.Không màu, không mùi.
C.Tan nhiều trong nước.
D.Nhẹ hơn không khí.
Câu 2: Để phân biệt axetilen và metan người ta dùng
A.dd AgNO3.
B.dd NaOH.
C.dd Ca(OH)2.
D.dd brom.
Câu 3: Phương trình hóa học nào sau đây không đúng?
A. C2H2+ Br2→ C2HBr + HBr
B. 2C2H2 + 5O2
C. CaC2 + 2H2O → C2H2 + Ca(OH)2
D. C2H2+ 2Br2 → C2H2Br4
Câu 4: Ứng dụng nào sau đây là của axetilen?
A. Làm nguyên liệu để sản xuất nhựa PVC
B. Dùng làm nhiên liệu trong đèn xì oxi – axetilen để hàn cắt kim loại.
C. Làm nguyên liệu để sản xuất cao su, axit axetic.
D. A, B, C đều đúng.
Câu 5: Khối lượng khí O2 cần dùng để đốt cháy 2,24 lít khí axetilen ở điều kiện tiêu chuẩn là
A. 8 g
B. 16 g
C. 4g
D. 32 g
Hướng dẫn giải và đáp án bài tập luyện tập
ĐÁP ÁN
1C | 2D | 3A | 4D | 5A |
Câu 5:
PTHH: 2C2H2 + 5O2
TL: 2 5 mol
Phản ứng: 0,1 0,25 mol
Giáo viên biên soạn: Ông Thị Tuyết Thanh
Đơn vị: Trường THCS và THPT Nguyễn Khuyến
