Bộ Y tế Canada xác nhận Pfizer và đối tác BioNTech đã cung cấp dữ liệu sơ bộ về thử nghiệm vaccine phòng Covid-19 cho trẻ từ 5-11 tuổi lên bộ này sớm hơn dự kiến.
Trước đây, việc xin cấp phép cho vaccine của Pfizer đối với người lớn cần khoảng 2 tháng kể từ khi bắt đầu nộp hồ sơ lên Bộ Y tế Canada.
Hiện Canada chưa cấp phép bất kỳ vaccine phòng Covid-19 nào dành cho trẻ dưới 12 tuổi, do đó, việc phê duyệt vaccine cho trẻ từ 5-11 tuổi sẽ là một bước tiến lớn.
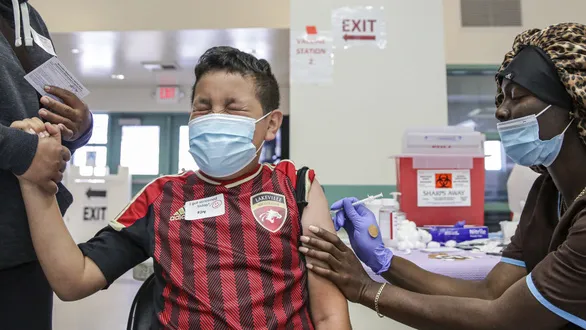
Pfizer cho biết trong quá trình thử nghiệm, số trẻ em trong độ tuổi 5-11 được tiêm liều vaccine chỉ bằng 1/3 liều tiêm dành cho người lớn.
Tuần trước, người đứng đầu Cơ quan y tế công cộng Canada Theresa Tam nhấn mạnh an toàn là ưu tiên hàng đầu đối với việc tiêm chủng cho trẻ em. Cho đến nay, chương trình tiêm chủng cho trẻ trong độ tuổi từ 12-17 đang đạt kết quả tốt. Việc xem xét các dữ liệu an toàn ở trẻ em dưới 12 tuổi là vô cùng quan trọng.
Tại Hoa Kỳ, dữ liệu của Pfizer thu được từ thử nghiệm với 2.268 trẻ trong nhóm tuổi dưới 12 tuổi này, với liệu trình tiêm hai liều cách nhau 21 ngày.
Trong thử nghiệm này, trẻ từ 5-11 tuổi được tiêm liều vắc xin 10 mcg, ít hơn so với liều 30 mcg được dùng để tiêm cho người từ 12 tuổi trở lên.
Phản ứng miễn dịch của nhóm trẻ tham gia thử nghiệm được đo bằng mức kháng thể trung hòa trong máu, và so với mức kháng thể trung hòa của nhóm người từ 16-25 tuổi đã tiêm hai liều, với mức 30 mcg/liều.
Pfizer và BioNTech khẳng định vắc xin của họ "an toàn, dung nạp tốt, cho phản ứng kháng thể trung hòa mạnh mẽ" với nhóm trẻ từ 5-11 tuổi.
Trước đó ngày 28/9, Pfizer và BioNTech cho biết họ có kế hoạch nộp dữ liệu cho Cơ quan Dược phẩm châu Âu và các cơ quan quản lý khác. Đồng thời cũng sẽ nộp dữ liệu đầy đủ về kết quả thử nghiệm lâm sàng giai đoạn ba để giới khoa học bình duyệt.
Giới chức Cơ quan Quản lý thực phẩm và dược phẩm Hoa Kỳ (FDA) cho biết sau khi nhận đủ dữ liệu thử nghiệm, cơ quan này có thể cấp phép vắc xin cho trẻ nhỏ hơn trong vòng vài tuần chứ không phải vài tháng. Song, điều này phụ thuộc vào thời gian và chất lượng của dữ liệu đã nộp.
Trước đây FDA đã nhanh chóng cấp phép sử dụng vắc xin cho các nhóm tuổi khác. Ví dụ, ngày 9/4, Pfizer nộp đơn xin cấp phép vắc xin cho trẻ từ 12-15 tuổi, thì tới ngày 10/5, FDA đã cấp phép khẩn cấp cho vắc xin này.
Tuy nhiên, với nhóm trẻ nhỏ hơn, FDA sẽ phải triệu tập ban cố vấn vắc xin để nghe khuyến nghị trước khi cấp phép.




